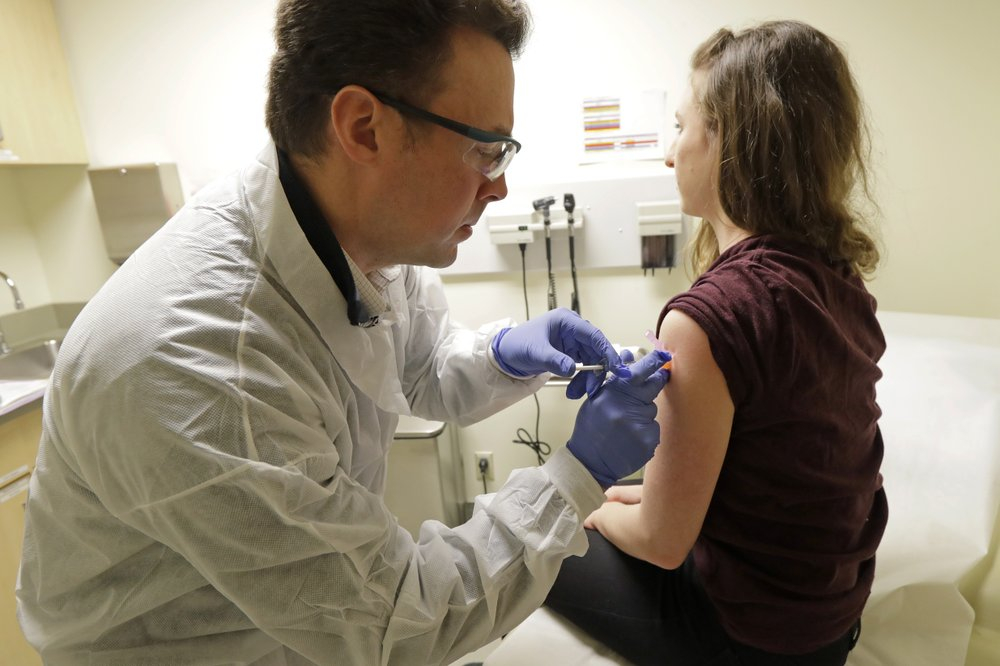
Участники исследования говорят, что прививки не более болезненные, чем обычная вакцина против сезонного гриппа. Некоторые получат более высокие дозы, чтобы проверить, насколько сильной должна быть доза. Также у них проверят наличие побочных эффектов и возьмут анализ крови, чтобы определить, повышает ли вакцина иммунную систему.
Волонтеры – это 43-летняя менеджер по операциям в небольшой технологической компании Дженнифер Халлер, 46-летний сетевой инженер в Microsoft Нил Браунинг и 25-летняя Ребекка Сирулл, редактор-координатор в независимом глобальном исследовательском центре здравоохранения в Вашингтонском университете. Все трое работают из дома, чтобы замедлить распространение COVID-19.
«Мы все чувствуем себя такими беспомощными. Для меня это удивительная возможность что-то сделать », - сказала Дженнифер Халлер.
Сирулл присоединилась к исследованию вакцин, чтобы «внести позитивный вклад в ситуацию»,
«Вы знаете, основные руководящие принципы, которые у нас сейчас есть, - оставаться дома и ничего не делать, что является довольно трудным посланием, чтобы услышать», - отмечает она.
На сайте National Institutes of Health указывается, что первая фаза клинических испытаний вакцины, разработанной для защиты от коронавирусной болезни 2019 года (COVID-19), началась в Вашингтонском научно-исследовательском институте здоровья Kaiser Permanente (KPWHRI) в Сиэтле. Вакцина называется мРНК-1273 и была разработана учеными NIAID (Национальный институт аллергии и инфекционных заболеваний) и их сотрудниками в биотехнологической компании Moderna, Inc., расположенной в Кембридже, штат Массачусетс. Всего в открытом исследовании будут участвовать 45 здоровых взрослых добровольцев в возрасте от 18 до 55 лет в течение примерно 6 недель. Это исследование – важный первый шаг на пути к предотвращению заражения новым коронавирусом. В настоящее время нет утвержденных вакцин.
Исследовательская вакцина направляет клетки организма на экспрессию вирусного белка, который, как надеются ученые, вызовет сильный иммунный ответ. Вакцина мРНК-1273 показала себя многообещающе на животных, и это первое испытание на людях.
Участники исследования получат две дозы вакцины путем внутримышечной инъекции с интервалом приблизительно 28 дней. Каждому участнику будет назначено получение дозы 25 мкг (100 мкг), 100 мкг или 250 мкг при обеих прививках, по 15 человек в каждой когорте дозы. Первые четыре участника получат одну инъекцию с низкой дозой, а следующие четыре участника получат дозу 100 мкг. Исследователи изучат данные о безопасности перед вакцинацией оставшихся участников в группах доз 25 и 100 мкг и до того, как участники получат свои вторые прививки. Еще один анализ безопасности будет сделан до того, как участники будут зачислены в когорту по 250 мкг.
Клиницисты будут контролировать участников на предмет общих симптомов вакцинации. Команда протокола будет регулярно встречаться для проверки данных по безопасности, а комитет по мониторингу безопасности также будет периодически просматривать данные испытаний и давать рекомендации NIAID. У участников также возьмут образцы крови в определенные моменты времени, которые исследователи будут тестировать в лаборатории для выявления и измерения иммунного ответа на экспериментальную вакцину.