Пандемия коронавирусной инфекции подарила нам мРНК-вакцины, и теперь на основе этой новой технологии ученые разрабатывают прививки от других вирусов, в том числе от гриппа, ВИЧ и даже рака. Вирусолог и волонтер Medsupportkz Асель Мусабекова рассказывает обнадеживающие новости из мира науки.
Вы можете прочитать текст или послушать подкаст:
Давайте поговорим о том, зачем нам в принципе нужны разные виды вакцин. Мы встречаем тысячи различных патогенов и инфекций, но мы не должны паниковать от этой мысли, потому что человечество всегда живет вместе с ними. Наша иммунная система обучена отвечать на большинство инфекций, и мы даже не замечаем, как она с ними справляется. Но некоторые инфекции особо опасны и требуют вакцинации, соответственно, мы развешиваем везде портреты этого «особо опасного преступника» и предупреждаем всех, что вот его особенно нужно бояться и для него необходимо сформировать спецназ. Вакцина является таким портретом, предупреждающим нашу иммунную систему, и она заранее формирует бойцов в виде специфических антител и специальных клеток-убийц, и, таким образом, когда мы заболеваем — видим преступника, — мы сразу же выпускаем спецназ.
Раньше для этого у нас были традиционные подходы — живые вакцины. Например, есть вакцина от туберкулеза — БЦЖ, которой уже больше 100 лет. Мы берем инфекцию, будь то бактерия или вирус, а потом её ослабляем за счет того, что выращиваем очень-очень много раз в лаборатории, и этот ослабленный вирус или бактерию используем в качестве вакцины. Так сделаны прививки от кори, ветрянки, туберкулеза. Затем около 70 лет назад у нас появилась другая технология: инактивированные вакцины. Таким же образом мы выращиваем наш патоген, инфекцию, а затем убиваем её, обычно это делается химическим агентом, вроде, например, формальдегида, который использовался в отечественной вакцине от коронавируса QazVac. Этот убитый патоген мы используем как вакцину. Это два традиционных подхода, которые, в принципе, помогали нам справляться с основными детскими инфекциями. Но у них есть недостатки: во-первых, для производства вакцины нужен сам вирус или бактерия, а они достаточно опасны, поэтому нам необходимы лаборатории высокой степени биобезопасности. Во-вторых, вирусы нужно выращивать в больших количествах, для этого необходимы реакторы и люди, которые обучены работать с такого рода патогенами. Это всё дорого и занимает очень много времени.
Что такое мРНК-вакцина
На протяжении ста лет молекулярная биология менялась, и сейчас есть технологии, которые позволяют нам менять геном, то есть менять код РНК или ДНК так, как мы хотим, называется эта технология генетические ножницы или CRISPR-Cas9, её авторы получили Нобелевскую премию. У нас так же есть технологии, благодаря которым в лаборатории с помощью простого химического синтеза мы можем составлять сами эти молекулы, кодировать генетическую информацию так, как нам это нужно. У нас также появились технологии, позволяющие модифицировать эти генетические молекулы и делать так, что некоторые их свойства будут более выражены, а некоторые — менее. Со всеми новшествами в молекулярной биологии мы пришли к пандемии, и она стала толчком для использования этого научного прогресса.
Часто думают, что мРНК вакцины — новая технология, появившаяся во время пандемии. Однако сама технология разрабатывалась еще с 80-х годов, тогда ученые начали рутинно синтезировать молекулы мРНК, а затем поняли, что их можно каким-то образом модифицировать, и уже с 1993 года работают над тем, чтобы сделать из этой молекулы лекарство. Для этого нужно, чтобы мы могли это лекарство доставить до необходимых нам клеток, чтобы эти молекулы могли нормально выводиться из организма и мы могли бы за этим следить и т.д. В принципе, с 1993 года мы работаем над этим очень плотно. Благодаря пандемии в мире появилась первая мРНК-вакцина
Перед тем, как поговорить о ее преимуществах, нужно вспомнить про векторные вакцины, такие как «Спутник» «Астра Зенека», потому что они — что-то среднее между традиционными подходами и мРНК-вакцинами. Как понятно из названия, в векторных вакцинах есть вектор, — другой вирус, грубо говоря, каркас, еще можно сказать, что это транспорт для того, чтобы взять и перенести нужную нам клетку, генетическую информацию, которая кодирует частичку вируса или бактерии. Мы используем в качестве вектора знакомые нам вирусы, такие, как, например, аденовирусы. Это простудные вирусы, с которыми мы знакомы, они не вредны. Мы знаем, как наша иммунная система будет с ними справляться, но здесь есть такая опасность: мы можем уже иметь иммунитет на этот вектор, и тогда вакцина может быть не такой эффективной, как нам хочется. И мРНК-вакцины — это третий шаг в этой эволюции вакцинологии, потому что здесь мы избавляемся от всего лишнего, даже от этого вектора. Для векторных вакцин нам тоже нужны лаборатории, которые будут выращивать вектор и т.д. Производство мРНК-вакцин — уже совершенно другой процесс. Это очень чистый, очень понятный, логичный и быстрый химический синтез определенных молекул, которым мы задаем программу. То есть, мы хотим, чтобы у нас была мРНК, которая кодирует белок-шип коронавируса, именно эту его часть, потому что на нее образуются очень хорошие антитела, и мы этот кусочек вставляем, и нам нужно эту молекулу упаковать, потому что мРНК-молекула очень хрупкая. Как вы знаете, для мРНК-вакцин нужно покупать холодильники на температуру минус 70-78 градусов, это связано с тем, что молекулы очень хрупкие, мы не можем просто взять, положить раствор с мРНК-молекулами и колоть шприцем. Нам необходимо эти РНК упаковать в упаковку из липидных наночастиц для того, чтобы они могли дойти до той клетки, где нам нужно, зайти в клетку и там уже превращаться в необходимый нам белок, выставлять его на поверхность клетки и вырабатывать на это всё иммунитет.
мРНК упакована в липидную наночастицу. Это такой очень маленький мыльный пузырь, который позволяет этой молекуле РНК безопасно дойти до клетки, зайти в нее и т.д.
Какие есть преимущества у этой технологии? Уменьшается стоимость и время производства, повышается безопасность, потому что мы не используем ни бактериальные клетки, ни клетки человека, чтобы выращивать вирус. Нам не нужно строить огромные лаборатории биобезопасности и покупать реакторы. При этом повышается чистота продукта. Мы знаем намного больше о том, что находится в составе мРНК-вакцин, чем когда мы использовали традиционные подходы. Ведь очистка традиционной вакцины — это тоже довольно серьезный процесс. Здесь же очень много контроля в руках человека, и, конечно же, точность того, что именно мы хотим, чтобы клетка производила. И мы можем менять этот код, то есть эти буквы, в зависимости от того, как будет меняться вирус, если мы говорим о мутациях, как заболевание будет меняться, если мы говорим о вакцинах от рака и т.д. Мы можем сделать какую-то платформу, с какой-то определенной упаковкой, которая придет в определенные клетки и будет делать эту работу.
мРНК-технология дает нам свободу, технология адаптируется под наши нужды. И вот это все есть преимущество технологии мРНК-вакцин, которые, наконец, мы использовали во время пандемии. Наконец — потому что появились деньги, мотивация, компании, которые решили вкладываться в третью фазу, и таким образом мы использовали эту технологию в вакцинах и видим, что это технология будущего.
Правда ли, что мРНК-вакцины внедряются в ДНК человека и изменяют его?
Эта технология в принципе никак не соприкасается с нашим собственным геномом. Есть наша клетка, у нее внутри ядро — отдельная структура в клетке, довольно защищенная. Я люблю сравнивать это с красивой книгой рецептов, которая, допустим, у вас есть. Вам очень жалко ее носить с собой на кухне, и вы ее оставляете на полке. Эта книга рецептов — это ДНК, она находится в ядре, на полке, никто ее не трогает, она защищена и очень мало меняется. Затем мы хотим приготовить одно блюдо — например, яблочный пирог с корицей. Для этого я беру обычный листок и из этой красивой книги переписываю этот рецепт, эту бумажку беру с собой на кухню и готовлю свой пирог. Так вот, этот рецепт — это мРНК.
То есть, когда нам нужен один конкретный белок, нашей клетке дали задание и у нас в ядре образуется именно эта мРНК, потом она выходит из ядра в саму клетку, и там уже в этой более-менее свободной жидкости мРНК превращается в конкретный белок. То есть, наш рецепт, переписанный из книжки на листочек, прекращается в яблочный пирог. А яблочный пирог — это конечный продукт, это белок.
Соответственно, мРНК-вакцина попадает в клетку, но не вовнутрь ядра, она остается в этой жидкости, там, где сразу превращается в белок. То есть, мы опускаем этот первый шаг с ДНК, с нашей библиотекой, с нашей книжкой, мы сразу же пришли в то место, где будет образовываться белок. мРНК не заходит в ядро, она в принципе физически не может этого сделать, нет такого механизма, она физически с нашей ДНК не соприкасается вообще. Есть некоторые РНК-вирусы, которые интегрируются в ДНК, очень хороший пример — вирус иммунодефицита человека. У ВИЧ-РНК, которая заходит в нашу клетку, превращается потом в ДНК с помощью определенной реакции и с помощью еще одного белка, который называется интеграза, она интегрируется в нашу ДНК. То есть для этого ей нужно очень много ресурсов.
У векторной технологии тоже нет такой возможности интегрироваться, но у нее есть возможность зайти в ядро, мРНК-технология является намного более безопасной в этом аспекте.
Можно ли сказать, что будущее за тем, что все вакцины будут уже сделаны на основе РНК?
Наверное, это будущее, которое нас ждет. Потому что эта технология удешевит процесс. Смотрите, почему нам нужны новые вакцины, почему мы сталкиваемся сейчас с пандемией? Ответ тут философский: это увеличение количества человек на земле, перенаселение. Почему пандемия началась в Китае? Потому что там человечество наступает на территорию дикой природы, начинает с ней коммуницировать и получается пандемия. В таких ситуациях нам нужны технологии, которые нам позволят адаптироваться, быть очень быстрыми и реагировать на такие ситуации. И это касается, например, вируса Зика, который может повлиять на ребенка, находящегося в утробе матери. Сейчас как раз разрабатывается мРНК-вакцина против этого вируса. То есть, речь не только о старых патогенах. Да, у нас есть живая вакцина от кори, краснухи, паротита, БЦЖ от туберкулеза, которая далеко не идеальна, — к сожалению, она не защищает от заражения, иначе бы у нас в стране не было бы туберкулеза. Она защищает от тяжелых осложнений и последствий, от смерти в первые пять лет жизни и, собственно, на этом всё. К тому же очень тяжело с помощью традиционных подходов сделать эффективную вакцину, и здесь вся надежда на технологию мРНК. Давайте посмотрим на кандидатов на мРНК-вакцину: вирус Зика, бешенство, грипп, цитомегаловирус, респираторно-синцитиальный вирус — очень заразная инфекция, от которой страдает много детишек — это тот самый бронхиолит — кашель, так сильно пугающий родителей. Боррелиоз или болезнь Лайма — инфекция, передающаяся клещами. У нас нет вакцин от этих болезней, потому что мы просто не могли их сделать.
Эта прекрасная новость появилась отчасти благодаря пандемии коронавирусной инфекции.
Почему так сложно разработать вакцину от ВИЧ
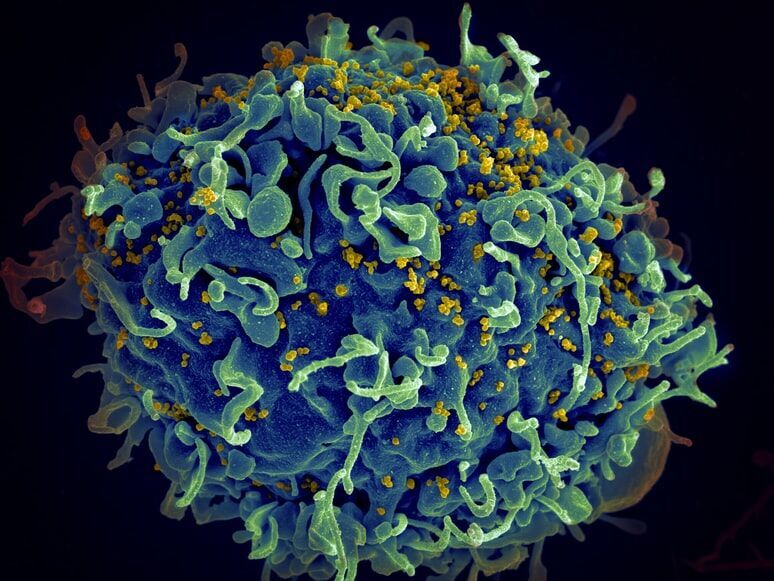
ВИЧ — очень хитрый вирус по нескольким причинам. Первая проблема в том, что, как мы уже сказали, вирус может интегрироваться в ДНК, то есть становится частью нас, нашего генома. То есть живую вакцину мы сделать не можем. Вторая проблема состоит в том, что ВИЧ меняется с огромной скоростью. По сравнению с ним коронавирус мутирует очень медленно, несмотря на то, что нас постоянно пугают все эти заголовки про новый вариант. Между уханьским вариантом и омикроном разница меньше, чем разница между двумя вирусами ВИЧ в одном пациенте. То есть, будучи в одном человеке, вирус ВИЧ мутирует с такой скоростью, что мы просто не успеваем его поймать. Проблема в том, что на его поверхности есть такие гликопротеины, — оболочка вируса сделана из этих белков, и они очень сильно мутируют, меняются, мы просто не успеваем понять, что же есть наша мишень, что же мы можем использовать в качестве вакцины. Еще существует генетическое разнообразие этих вирусов в зависимости от того, где они. То есть, ВИЧ в Африке и ВИЧ в США — это, условно говоря, отдельная ветка эволюции. Затем есть такая еще проблема: так как вирус интегрируется, то, возможно, антительные ответы не будут срабатывать так хорошо, как против других патогенов. Но есть другая часть нашего иммунитета — Т-клеточный иммунитет. Он является загадкой, потому что мы знаем, что он защищает нас от тяжелых последствий, мы знаем, что Т-клеточный иммунитет возникает после вакцинации некоторыми вакцинами (не всеми) — традиционные подходы практически не дают Т-клеточный иммунитет, только его минимальный уровень.
И вот здесь мы понимаем, что против ВИЧ важен Т-клеточный иммунитет. То есть нам нужны вакцины, которые дадут нам Т-клеточный иммунитет, но ВИЧ как раз-таки инфицирует эти самые Т-клетки и путает всю эту систему защиты. То есть, почему ВИЧ — вирус иммунодефицита? Потому что он, заражает клетки иммунной системы, и она настолько запутывается, что мы не понимаем, какие клетки за нас, а какие клетки против нас.
И именно этот кусочек закодирован в мРНК-вакцине, которая используется в первой фазе клинических испытаний. Заявила об этом компания Moderna, потому что сама лаборатория не в силах сделать полностью этот продукт для клинических испытаний. Поэтому Moderna здесь помогает своей платформой. Эта генетическая информация будет использована на такой же платформе, что и вакцина от коронавирусной инфекции, то есть, упаковка такая же — липидная наночастица, и Moderna поможет провести это испытание, потому что это тоже стоит денег.
В первой фазе испытаний будут участвовать 56 человек — все ВИЧ-отрицательные, ученые будут изучать, что происходит с вакциной в организме, как на нее люди реагируют и т.д. Важно понимать, что эта первая фаза нам не скажет, работает ли вакцина. Здесь мы вспоминаем историю с QazVac, где третья фаза до сих пор, к сожалению, нигде не опубликована, но мы везде видим рекламные баннеры про 96% эффективности. Первая и даже вторая фаза ничего нам об эффективности не скажет.
Одна мРНК-вакцина от гриппа на всю жизнь
У нас есть огромные организации, институты, которые каждый год изучают, какой же штамм гриппа будет циркулировать в новом сезоне. Особенность вируса гриппа состоит в том, что он как лего — у него есть несколько вариантов сочетания комбинации антигенов (белков) на поверхности. То есть, его упаковка меняется каждый год, поэтому прошлогодняя вакцина работать в этом году не будет. Сейчас уже есть тривалетные, четырехвалетные вакцины от гриппа, потому что чем больше у нас штаммов включено в состав вакцины, тем больше вероятность, что мы попадем именно в тот штамм, который будет циркулировать, но попадаем мы не всегда. То есть, эффективность вакцины от гриппа варьируется от 30 до 70%.
Ученые уже лет 20 активно думают над вопросом: есть ли какой-то универсальный антиген, то есть часть вируса гриппа, которая никогда не меняется? Эту часть можно закодировать и сделать в виде вакцины, которая будет защищать нас сразу от всех штаммов. То есть нам позарез нужна универсальная вакцина от гриппа, и, конечно, мРНК-технология здесь тоже очень привлекательна, потому что она позволяет нам очень специфически выбирать частичку генома и синтезировать её в такой форме, в которой мы хотим. Мы можем сделать такую вакцину, что она приведет к производству белка именно в определенной форме. И бывает такая конформация (форма белка), на которую антитела реагируют. А бывает такая, на которую ничего не будет реагировать. Вот это все мы можем продумать при мРНК-технологии. И мы можем выбрать кусочек вируса гриппа, который при определенной конформации будет как бы выставлен наружу, и он будет постоянный, общий для всех штаммов, универсальный. Это священный Грааль всех разработок. Это и есть цель для мРНК-вакцины, поэтому так много желающих попробовать эту технологию. Если все получится, то одной прививки нам будет достаточно, чтобы защититься от всех штаммов гриппа, не нужно будет делать это каждый год.
Вакцина от герпесвирусов
Моя магистерская диссертация была именно про герпесвирусы. Когда наш знаменитый казахстанский ученый Кен Алибек, который сейчас в США, был в Назарбаев университете, мы под его руководством работали над этим проектом — универсальной вакциной против семейства герпесвирусов, это был академический проект, не связанный с фармакологией. Это просто были наши размышления о том, как можно использовать биоинформатику для того, чтобы сделать универсальную вакцину против герпесвируса. Вирус Эпштейна-Барра является частью этого семейства герпесвирусов, к нему так же относится простой герпес — тот, что вылезает на губах, генитальный герпес, затем цитомегаловирус, который может повредить мозг ребенка в утробе матери, если она впервые заболеет им во время беременности. Помните, что когда мы видим антитела к нему и к вирусу Эпштейна-Барра, лечить их бесполезно. Если вы теряетесь, когда ЦМВ и ВЭБ нужно лечить, а когда не нужно, рекомендую блог инфекциониста Дарьи Паниевой. К сожалению, врачи, придерживающиеся недоказательной медицины, при наличии антител к этим заболеваниям, очень любят отправлять людей лечиться. Но, тем не менее, эти вирусы довольно опасные. К этому же семейству относится ужасно противный вирус ветрянки. Против нее есть хорошая вакцина, которая недоступна в Казахстане. Эта вакцина не должна быть какой-то роскошью, она должна быть в прививочном календаре любой цивилизованной страны. Ветрянка не так безобидна, как мы думаем. Мы организовываем «ветряночные вечеринки», а потом вирус засыпает в нашем организме и просыпается в самый неподходящий момент, когда происходит сильный стресс, возрастает нагрузка на иммунитет, нас атакует несколько разных инфекций. Вирус ветрянки в опоясывающем лишае, который очень тяжело переносится.
В чем же проблема со всем этим семейством герпесвирусов? Дело в том, что это ДНК-вирусы, одни из самых больших вирусов, если мы посмотрим на их размер и на размер их генома: в нем огромное количество генетической информации. Группа герпесвирусов очень тесно эволюционировала вместе с человеком. В нашем геноме, в нашем ДНК есть частички герпес-вирусов, и в геноме герпесвирусов есть наши собственные гены. Это приводит к тому, что эти вирусы очень успешно могут прятаться в нашей иммунной системе. Есть стадия активной инфекции: лихорадка, воспаление, то есть, есть симптомы. Затем вроде бы мы вылечились, вот у нас вылезает герпес на губе, мы помазали мазью ацикловир, но он же в следующий раз опять вылезет. Мы от вируса не избавились, потому что он прячется. Так, например, вирус Эпштейна-Барра любит клетки иммунной системы, цитомегаловирус — клетки мозга, он даже может быть фактором возникновения рака мозга. Они спокойно сидят, наша иммунная система их просто не видит.
Еще проблема в том, что вирусы вызывают так называемое иммунное старение. Когда мы стареем, наша иммунная система тоже стареет. У нас энное количество наивных клеток, которые никогда не видели патогена, и они сидят готовые, чтобы из наивных превратиться в обученных. И когда мы стареем, у нас остается меньше наивных клеток иммунной системы и больше обученных, то есть мы добавляем себе иммунную память, но, тем не менее, у нас страдает наша реактивность. Поэтому старческий возраст является фактором риска при гриппе: у нас меньше наивных клеток, и мы медленнее реагируем на вирус. Цитомегаловирус все эти иммунные наивные клетки забивает своими антигенами. К примеру, если мы возьмем все Т-клетки определенного типа и посмотрим на то, на какие антигены они реагируют, то увидим, что вот эта клетка запомнила корь, а вот эта — грипп, а потом замечаем, что 70% этих клеток у нас заполнил цитомегаловирус. То есть он берет и забивает иммунную память своими антигенами, и такое ощущение, что он делает это специально, потому что это приводит к инфляции иммунной памяти. Грубо говоря, снижается стоимость нашей иммунной валюты, и это приводит к иммунному старению.
Из-за всех этих сложностей, из-за того, что вирус так активно прячется от иммунной системы, мы не можем использовать традиционные подходы вакцинологии. Поэтому в данном случае РНК-технология может нам дать какую-то надежду на то, что мы можем справиться с этими вирусами. И здесь очень важно, что есть вакцины, которые спасают от первичного заражения, и так же есть препараты, которые защищают нас от реинфекции — когда инфекция просыпается. Речь о двух разных вакцинах: от ветрянки и от опоясывающего лишая. Когда мы говорим о подходах в использовании мРНК-вакцин против герпесвирусов, таких как ЦМВ и ВЭБ, мы имеем в виду два варианта: защиту от заражения и защиту от реактивации. Реактивация потенциально может стать очень большой проблемой для людей, у которых есть какая-то иммуносупрессия. Например, очень часто вирус Эпштейна-Барра и цитомегаловирус становятся опасными для людей после трансплантации, — если в такой ситуации проснется ЦМВ, он может навредить достаточно прилично. В таких ситуациях, например, нам бы не помешала мРНК-вакцина, которая бы помогала нам от реактивации. Вот такие очень конкретные задачи стоят перед учеными и врачами.
Вакцина от рака
Давайте поймем, почему есть такое понятие, как вакцина от рака. Очень многие люди не знают о том, что наша иммунная система защищает нас не только от вирусов, бактерий, паразитов, грибов и т.д. Она так же защищает нас от наших собственных клеток, которые могут превращаться в раковые. В нашем организме постоянно возникают раковые клетки. Наша иммунная система обучена находить и убивать такие клетки: на поверхности этих клеток есть специфические антигены, то есть специфические молекулы, которые являются маркером, сигналом. Но иногда иммунная система упускает момент, она не увидела вовремя эту раковую клетку, и, к сожалению, появляется опухоль. Клетка начинает так много делиться, что уже формирует огромное количество клеток, которые превращаются в опухоль. По сути, рак — это болезнь иммунной системы. Человек болеет, потому что иммунная система упустила этот сигнал. Как мы можем с этим бороться? Вакцины от рака могут быть превентивными, профилактическими — до того, как человек заболел. Например, это вакцина от вируса папилломы человека (ВПЧ), вакцина от вируса гепатита В. К сожалению, в Казахстане вакцины от ВПЧ сейчас нет, но я надеюсь, что она будет, ведь она защищает нас от рака шейки матки и других раков, от рака головы и шеи, в том числе у мужчин. Вакцина от гепатита В защищает нас от рака печени.
Также есть другая категория — это вакцины терапевтические, то есть, когда человек уже заболел, и мы хотим ввести определенную молекулу, которая будет вести себя как вакцина и поможет человеку справиться с раком или сможет остановить его рост или метастазы. Продлить его жизнь, улучшить качество жизни, и, что немаловажно, качество его смерти. мРНК-вакцины мы можем использовать именно для того, чтобы сделать копию этих специфичных раковых антигенов, которые подают сигнал нашей иммунной системе — чтобы она чуть-чуть поактивней начала реагировать, была уже в состоянии пробуждения, чтобы она реагировала более активно, и, скажем, предотвращала возникновение метастаз. Здесь есть два подхода. Первый: использовать те антигены, которые специфичны для определенного вида рака. Мы знаем, что видов рака огромное множество, и соответственно, эти сигналы, которые рак подает иммунной системе, они могут быть разные.
На самом деле сфера использования мРНК-вакцин началась с рака, а не с инфекций — именно для борьбы с онкологией изначально были придуманы мРНК-вакцины.
Например, возьмем исследование, которое призвано вылечить рак простаты, оно уже дошло до второй фазы, это значит, что уже показали, что вакцина достаточно безопасна, и сейчас мы смотрим на то, насколько она приводит к определенному виду иммунитета. Это уже вторая фаза, в ней участвуют сотни человек. И там использовалась комбинация из четырех антигенов именно специфичного рака простаты, то есть нам сначала нужно хорошо продиагностировать человека, понять, что в этих клетках на самом деле присутствуют эти специфические антигены именно этого вида рака, и лечить уже вот этой вакциной, чтобы нашу иммунную систему разбудить.
Напоминаю, что это первый подход, и он уже дошел до второй фазы испытаний. Третьей фазы испытаний на раковых больных нет, потому что это тяжело, есть определенные этические нормы, что и когда мы можем использовать в качестве лечения, что нет. Это терапия для терминальных больных, когда им уже не помогают традиционные технологии, и тогда мы можем использовать новые генетические технологии. Изучение вакцины от рака происходит достаточно медленно из-за этических норм. Ведь когда у нас есть человек, умирающий от рака, его нужно лечить тем, что нам знакомо. К первоначальным исследованиям допускают только терминальных больных, у которых нет большого выбора.
Второй подход: персонализированная мРНК-терапия. Это, например, когда у нас есть определённый вид рака и мы знаем, что у человека сейчас идет тенденция к тому, что будут метастазы, мы берем и смотрим клетки именно его рака, находим там антигены, которые именно на поверхности его клеток, и из этих антигенов мы варим эту мРНК-вакцину. Это то будущее персонализированной медицины, о котором мы говорили в нашем проекте Gylym Faces. Насколько я помню, была первая/вторая фаза испытаний, и речь шла о меланоме, имевшей тенденцию к метастазированию. Взяли 10 пациентов, у каждого из них отобрали их собственные раковые клетки и по ним сделали мРНК-вакцины. Эта история — не только о лечении раковых заболеваний как таковых, это в принципе будущее персонализированной медицины, когда мы можем очень быстро произвести очень технологичное лекарство для конкретного пациента. И здесь хочется сказать об аутоиммунных заболеваниях и аллергии. С помощью РНК-вакцин мы можем взять конкретного человека и конкретный аллерген, например, пыльцы, и понять, какая часть этого аллергена вызывает реакцию и использовать в качестве вакцины. То же самое, кстати, касается диабета первого типа, который является своего рода аутоиммунным заболеванием. И это для меня взрыв мозга, мы никогда не относились к фармакологии и к лечению таких заболеваний таким образом, чтобы можно было адаптировать систему под каждого пациента.
Поддержите журналистику, которой доверяют.